Problemă:
Un amestec de propan şi butan, ocupând un volum egal cu 10 ml, este supus arderii în exces de oxigen. După condensarea apei, de gazele rămase sunt trecute printr-o soluţie de KOH, volumul acestora reducându-se cu 36 ml. Determinaţi compoziţia în procente de volum a amestecului iniţial de hidrocarburi. (Volumele de gaze sunt măsurate în condiţii normale de temperatură şi presiune.)
Rezolvare
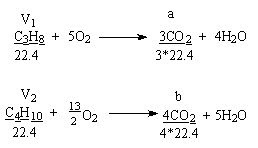
Ecuaţiile reacţiilor chimice:
KOH va reţine din amestecul de gaze rezultat după condensarea apei doar dioxidul de carbon, iar reducerea de volum de 36 ml este chiar volumul de dioxid de carbon rezultat din ardere.
V1 = volumul de propan
V2 = volumul de butan
a = volumul de CO2 rezultat din arderea propanului
b = volumul de CO2 rezultat din arderea butanului
Conform datelor problemei avem: V1 + V2 = 10 ml (1) şi
a+b =36 ml (2)
De pe ecuaţiile reacţiilor se obţine:
V1 = a/3 şi V2 = b/4, adică, înlocuind în relaţia (1) a/3 + b/4 = 10 (3).
Folosindu-ne de relaţia (2) vom obţine a = 12ml şi b = 24ml.
De aici, V1 = 4ml si V2 = 6 ml, iar
%C3H8 = 40%
%C4H10 = 60%
Iosif Schichetanz, Florin Badea - Chimie Organică prin probleme
Spunemi si mie te rog dc nu ai pastrat Ogixenul in reactie ca sa vina ceva de genul: KOH+O2--->CO2+H20
RăspundețiȘtergereÎn condiţiile date de problemă nu are loc reacţie între KOH şi excesul de oxigen. În condiţiile impuse de textul problemei, amestecul de gaze rezultat în urma arderii conţine dioxid de carbon şi oxigen neconsumat la ardere. Rolul hidroxidului de potasiu (KOH) este acela de a reţine dioxidul de carbon.
RăspundețiȘtergereCe rezulta in urma arderii unui amestec de CH4 si C3H4?
RăspundețiȘtergereCe rezultă în urma arderii CH4?
ȘtergereCe rezultă în urma arderii C3H4?
Ce rezultă dacă cele două hidrocarburi sunt amestecate şi ulterior arse?
Clar?
Succes!
cum se rezolva probleme cu exces?la cine iau excesul?la masa sau la volum?...cum se rezolva problema determina volumul de clor necesar pt clorurarea benzenului stiind ca s-a folosit un exces de 20% clor.avem reactia c6h6+3cl2 rezulta c6h6cl6+6hcl,benzenul are volumul 5L si densitatea 0,88 g/cm cub. trebuie sa dea volumul de clor 3,79 cm 3....multumesc anticipat
RăspundețiȘtergerePrima observaţie: reacţia este:
ȘtergereC6H6 + 6Cl2 ------------> C6H6Cl6.
Dacă îţi cere volumul de Cl2 necesar, nu te mai interesează excesul. Dacă autorul problemei ar fi vrut să foloseşti şi acel exces de 20% ar fi formulat textul de forma "Care este volumul de clor introdus în reacţia de clorurare a benzenului".
Transformă volumul de benzen în masă cu ajutorul densităţii, înlocuieşte pe reacţie şi ...
Succes!
Am si eu o problema ma puteti ajuta
RăspundețiȘtergere250 Kg dintr un carbun ce contine 85%carbon este ars in volum limitat de oxigen ce produs rezulta si in ce cantitate. Dar daca arderea are loc in exces de oxigen ce produs rezulta si in ce cantitate
RăspundețiȘtergereCe cantitate de metan trebuie arsa pentru a produce 448 l CO2 în condiții normale?
RăspundețiȘtergere