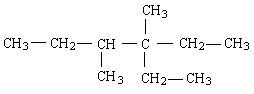
Alcanul din figura alăturată este de fapt un izomer al decanului(C10H22). Există reguli stabilite de catre IUPAC (International Union for Pure and Aplied Chemistry) care statutează modul în care se denumesc substanţele chimice, din diverse clase de substanţe. Pentru exemplul nostru, se procedeaza astfel:
1. Se identifică şi se numerotează catena cea mai lungă în ambele sensuri:
Se observă că aceasta este alcătuită din 6 atomi de Carbon, deci reţinem denumirea alcanului cu 6 atomi de carbon (HEXAN)
2. Se identifica atomii de Carbon la care se produc ramificaţii:
Aceştia sunt atomii de Carbon 3 şi 4.
3. Se identifică radicalii alchil de la atomii de carbon identificaţi mai sus.
Se observă că avem un radical etil şi doi radicali metil (doi radicali metil = dimetil)
Realizăm denumirea punând cap la cap informaţiile colectate la cei tri paşi anteriori:
- Pentru sensul numerotat cu albastru (de la stânga la dreapta): 4-etil-3,4-dimetil-hexan
- Pentru sensul numerotat cu roşu (de la dreapta la stânga): 3-etil-3,4-dimetil-hexan
3-etil-3,4-dimetil-hexan
Rămâne la latitudinea cititorului să stabilească dacă răspunsul elevului a fost sau nu perinent ("Presupun că se pronunţă altfel decât este scris...")